El misterio del supuesto militar que manejó la carrera de Elvis Presley y lo convirtió en el cantante más famoso de su época. ¿Quién era Tom Parker? ¿Era militar? ¿Era un agente encubierto de la CIA? O era simplemente un impostor.
Tal vez también te interese
Ekaterina gobernó un imperio las últimas tres décadas del siglo XVIII, Katalin y Kathrin hacen ciencia desde los años 80 del siglo XX. Estas Catalinas comparten haber nacido en la Europa que alguna vez fue socialista y hecho historia en centros de poder lejanos: tres inmigrantes. Separadas poco más de 150 años una vida de las otras, sin embargo, el tiempo las entrelaza con un delicado cordón de plata: cada una de ellas le ha plantado cara a las pestes de la humanidad.
Ekaterina II nació como Sophie Friederike Auguste von Anhalt-Zerbst en la actual Polonia (en el castillo prusiano de Stettin, Pomerania, hoy Szczecin). Hija de un noble de segundo nivel tuvo un casamiento muy oportuno en su adolescencia y, apenas treintañera, se convirtió en la emperatriz Catalina la Grande de Rusia, la mujer que rompió varios moldes en su época y agrandó los territorios hacia el este, el norte y el sur. Ella mantuvo firme el timón del imperio ruso durante 34 años hasta su muerte a los 67 en San Petersburgo, en 1796. Y fue la precursora de la vacunación en Rusia -el país donde surgió la vacuna Sputnik V- contra la gran peste de su tiempo, la viruela.

Katalin Karikó, húngara del pueblo de Szolnok, llegó al mundo en 1955, en tiempos de Guerra Fría y antes de que se levantara el Muro de Berlín en 1961, hija de un carnicero. Ya doctorada, a los 30 años dejó el Este con su esposo y una hija pequeña, hacia una beca de posgrado en Estados Unidos. Durante tres décadas investigó el ARN mensajero y soportó rechazos a sus investigaciones. Pero perseveró y triunfó. Hoy es vicepresidenta de BioNTech y se la considera la “madre” de la primera vacuna aprobada en el mundo contra el Covid-19.
Kathrin Jansen es alemana, nacida en Erfurt en 1958 , en la entonces República Democrática Alemana. Niña de salud frágil con afecciones a repetición en la garganta, logró salir con su familia hacia el Oeste antes de 1961, estudió microbiología al otro lado del Muro, a los 34 años ingresó a una farmacéutica líder e investigó ideas vanguardistas. Por largo tiempo chocó contra el escepticismo de sus pares y hoy, tras haber creado vacunas cruciales, la consideran una eminencia. Vive en Nueva York y lideró el desarrollo en tiempo récord de la vacuna de Pfizer/BioNTech.
Ekaterina rechazó en vida que la llamaran “la Grande”, el calificativo de admiración que la sobrevive; Katalin ha sido propuesta por varios colegas al Premio Nobel; Kathrin fue elegida por la revista Nature una de las diez figuras relevantes de la ciencia de 2020. Una, dos, tres Catalinas “grandes” que nacieron en sitios relativamente cercanos -noroeste de Polonia, sur de Hungría, centro de Alemania-, que bien podrían armar un triángulo con punta hacia abajo y se emplazan entre sí a una corta distancia de 476 a 1.064 kilómetros. Un capricho más de la Historia.
De la “variolización” en la época del imperio ruso al esperanzador paso actual del ARN, la humanidad dibujó una vuelta campana completa en su combate tenaz contra las enfermedades.
La variolización, el primer método para inocular contra la viruela, fue pre-vacuna y la inventaron los chinos. Tuvo dos fases: al modo oriental era por inhalación de materia orgánica infectada; más tarde, los británicos optaron por introducir el virus a través de un corte en el antebrazo.
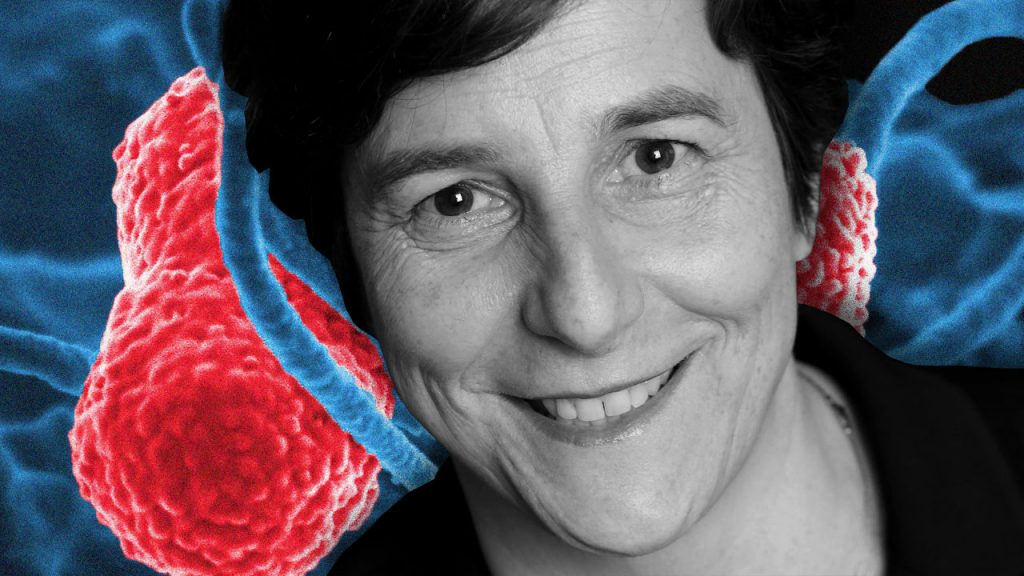
En el siglo XVIII atravesado por la viruela (sólo en Europa mataba a 400.000 personas por año y apenas Australia y algunas islas del Pacífico estaban por entonces libres del mal) la manera de “vacunarse” era algo cruenta y riesgosa. Dentro de la herida provocada por el corte se introducía un delgado hilo de seda con pus de un enfermo leve, con la esperanza de que el receptor se viera afectado también de forma leve y quedara inmunizado.
Pero podía fallar y entonces había peligro de muerte. A eso se arriesgó la emperatriz Ekaterina cuando convocó a su palacio de San Petersburgo al doctor Thomas Dimsdale, británico y pionero en el método, en 1768, un año después de que la viruela había matado a miles en la Siberia. Porque ella quiso ser la primera “vacunada” de “todas las Rusias”. Como contó en sus memorias:
“Mi objetivo era, a través de mi ejemplo, salvar de la muerte a la multitud de mis súbditos que, sin conocer el valor de esta técnica y asustados por ella, estaban en peligro”.
No muy convencido y temiendo un imperial fracaso, el doctor Dimsdale emprendió con su hijo el largo viaje de un mes a la capital rusa, intentó de mil maneras convencer a la emperatriz de comenzar con alguna otra persona, y -frente a la terca valentía de Ekaterina- inoculó primero a seis niños y una niña sanos y de uno de ellos, finalmente, extrajo materia orgánica infectada para cumplir su misión. Fue en octubre, de noche y en secreto: al chico elegido lo sacaron del hospital envuelto en una frazada mientras dormía y lo llevaron al palacio; la emperatriz fue inoculada en cada antebrazo. A la mañana siguiente, bajo un pretexto cualquiera, Ekaterina fue trasladada a su residencia veraniega para una cuarentena de tres semanas, durante la que tuvo moderada cantidad de pústulas por la enfermedad y logró finalmente la inmunización; el chico, retornado esa misma noche al hospital, también se recuperó y se ganaría un título nobiliario.
La noticia fue revelada recién al quinto día, y el éxito del procedimiento impulsó lo que Ekaterina quería, una inoculación masiva. Primero recibieron la variolización su hijo y toda la familia real, después unos 140 miembros de la nobleza, y más tarde la población común hasta alcanzar a unas 2 millones de personas. Aunque también entonces hubo, como sigue habiendo hoy, “antivacunas”. A ellos la emperatriz, que no las mandaba decir, les dedicó estas palabras: “Son verdaderos imbéciles, ignorantes o simplemente malvados”.

El médico británico y su hijo Nathaniel fueron recompensados con generosidad. Un título de barón del imperio ruso para cada uno, 10 mil libras por los servicios prestados, 2 mil más para gastos, y una pensión vitalicia de 500 libras al año.
Al cabo de un mes, y de haber organizado un hospital de inoculación también en Moscú, ambos debieron diferir su regreso a Gran Bretaña por una pleuresía que atacó a Ekaterina. Sólo retornaron a casa cuando la monarca estuvo completamente restablecida. El doctor Dimsdale volvería a Rusia una vez más, en 1781, para inocular a los nietos de la emperatriz, Alexander y Constantino.
Recién un buen tiempo más tarde, en 1796 (el año de la muerte de Ekaterina), Edward Jenner aplicaría a un niño la primera vacuna de la humanidad. Aquel logro del padre de la antivariólica y de la inmunología fue el hito decisivo contra la viruela, que perduró azotando casi dos siglos completos más y se declaró erradicada de la Tierra en días más cercanos, en 1980.
En un mundo ya sin viruela, en 1985, Katalin Karikó se la jugó y con toda decisión dio un vuelco a su vida: provocó su despido del Centro de Investigaciones Biológicas de la Academia Húngara de Ciencias, vendió el auto familiar en 1.200 dólares, escondió ese único capital en el peluche de su hijita (estaba prohibido sacar divisas de los países comunistas), cruzó la frontera y el Atlántico y se radicó con su esposo ingeniero en Pensilvania, Estados Unidos, con una beca de la Universidad de Temple, cuyo lema -dato no menor en su vida- es “La perseverancia triunfa”. Katalin rememoró hace poco que aquél “iba a ser un viaje de ida y no conocíamos a nadie”. Doctorada en bioquímica unos años antes en la Universidad de Szeged (la tercera ciudad de Hungría), ya estaba investigando sobre ácido ribonucleico; es decir, le venía contando las costillas al ARN.
Este ácido es el intermediario en el flujo de información genética, que se transmite en el sentido ADN-ARN-proteínas (las tres moléculas clave). El ácido ribonucleico le da a las células un “manual de uso” -instrucciones- para que puedan producir proteínas. En síntesis: el ARN es un “mensajero” de información genética.
Hace 40 años la ciencia occidental tenía los ojos puestos en el ADN (se lo veía como una esperanza contra el cáncer) y no en el ARN. Pero Katalin tenía la corazonada de que éste podía transmitir instrucciones a las células para que fabricaran proteínas terapéuticas por sí mismas. Así, pensaba, se evitaría modificar el genoma celular.

Los experimentos iniciales provocaron reacciones inflamatorias, el ARN mensajero era recibido como un intruso por el sistema inmunitario. Por esas inflamaciones hubo críticas a su trabajo, que estaba enfocado en apelar al ácido ribonucleico para tratar enfermedades (no a desarrollar vacunas). Y tuvo que enfrentar un momento crucial en 1990 cuando le rechazaron otra beca, en la Universidad en Pensilvania, donde ya estaba trabajando. No solo eso, la degradaron a investigadora simple y le rebajaron el sueldo (situación que aceptó para no perder su visa). “Normalmente, en este punto la gente dice adiós y se va. Y yo pensé en irme y hacer otra cosa. Me decía que no era lo suficientemente buena o inteligente”.
Pero no se fue. Hubo de soportar futuros nuevos rechazos de instituciones y farmacéuticas cuando les pedía dinero para el desarrollo técnico del ARN mensajero y, además, sexismo laboral: a pesar de que dirigía su propio laboratorio le preguntaban quién era su supervisor, o le decían “señora” cuando sus pares masculinos eran llamados “profesor”. Pero ella perseveró y se aferró a su pasión. “Visto desde afuera puede parecer loco, incluso insultante, pero era feliz en el laboratorio. Nunca dije `voy al trabajo´ porque siempre fue más un juego”.
Y su perseverancia tuvo frutos en 1997, junto a una fotocopiadora de la universidad. Un atasco de papel, una trivialidad bendita, le permitió conocer e iniciar una charla con el inmunólogo Drew Weissman (recién llegado a Pensilvania, venía del equipo de Anthony Fauci, eminencia en HIV y hoy al frente del instituto público norteamericano que co-desarrolló la vacuna de Moderna). Resultado del encuentro fortuito: Weissman, que buscaba una vacuna contra el HIV, creyó en la investigación de Katalin y comenzaron a trabajar juntos en un camino para que el sistema inmunológico no reconociera al ARN sintético. Como todo en la ciencia, les llevó su tiempo. Nueve años más tarde publicaron su trabajo, esta vez con buenas críticas. Y a partir de ese 2005 comenzaron a modificar el ARN con la molécula nucleósido, experimento que resultó en una vacuna “muy potente que no causaba inflamación y daba una respuesta inmune muy fuerte”, contó Katalin hace poco.
En 2010, un grupo de investigadores de Estados Unidos fundó una empresa que compró los derechos sobre las patentes de Katalin y Weissman. El nombre de la empresa incluía el acrónimo en inglés del ARN modificado: ModeRNA. Casi en simultáneo, una pequeña firma alemana fundada en 2008 por una pareja de científicos de raíces turcas -BioNTech- adquirió a su vez varias patentes de ARN modificado para desarrollar vacunas contra el cáncer. Tres años más tarde, Katalin fue contratada por BioNTech y hoy es su vicepresidenta senior.
En tanto, al cabo de otra década desde la primera publicación conjunta, en 2015 Katalin y Weissman lograron situar el ARN en nanopartículas lipídicas: un revestimiento que evita la degradación rápida y, a la vez, facilita el ingreso a las células. Ni más ni menos que el hallazgo clave que abrió la puerta a las vacunas de Pfizer y de Moderna.
La de Pfizer (la primera en ser aprobada: el 2 de diciembre último por Gran Bretaña) y también la de Moderna se basan en la introducción en el organismo de instrucciones genéticas para que el ARN mensajero les enseñe a las células a activar la producción de una proteína idéntica a la del Covid-19, y así se provoca una respuesta inmunitaria.
Katalin explica con total autoridad: “Se utilizaron ARN mensajero modificados con nucleósidos para crear las vacunas BNT162b2 de Biontech/Pfizer y ARNm-1273 de Moderna/NIH” (Institutos Nacionales de Salud-EE.UU.). Y remarca que “la vacuna de ARNm es más eficaz y segura que las vacunas clásicas, que contienen virus atenuados o inactivados”.

Estas dos vacunas -que ya se han aplicado a millones de personas desde diciembre- coronan el esfuerzo de su vida, y Katalin lo saborea: “Esto es algo increíble, porque significa que todo el trabajo que estuve realizando años enteros, durante la década del 90, y el convencer a la gente de que tal vez el ARNm sería bueno, valió la pena”.
Dice que “nunca” dudó de que “funcionaría”, porque había visto los resultados previos en animales de laboratorio. Aunque tenía un temor secreto: “Lo único que deseaba era poder vivir el tiempo suficiente para ver aprobado algo en lo que había trabajado durante años”. Jamás olvidará el día que se anunció el alto nivel de eficacia (90% en ese primer momento, 95% una semana después) de la vacuna de Pfizer/BioNTech. “Empecé a respirar muy fuerte. Estaba tan emocionada que sentí miedo a morir”.
Ese 9 de noviembre del anuncio científico que sacudió al mundo -un tubo de oxigeno contra el pesimismo mundial que marcó al 2020- alguien dijo en una entrevista: “Éste es un momento histórico”. Tenía razón Kathrin Jansen, jefa de Investigación y Desarrollo de Vacunas y vicepresidenta senior de la farmacéutica Pfizer. “Es una situación devastadora, una pandemia -agregó- y nos hemos embarcado en un camino y una meta que nadie ha logrado nunca, para llegar a una vacuna en el plazo de un año”. Hasta aquel día el Covid-19 había acabado con 1,2 millones de personas en el mundo (hoy las víctimas pasaron los 2 millones). Y jamás se había logrado una vacuna en menos de cuatro años.
El mojón inicial de la vacuna se colocó en Mainz, Alemania, a finales de enero de 2020. Ugur Sahin, director ejecutivo y cofundador de BioNTech, leyó sobre el virus en la revista británica The Lancet. Y sintió temor. “Casi instantáneamente supe que esto nos afectaría”, recordó Sahin en una entrevista. El mismo día se detectaron los primeros casos europeos, en Francia. Sin pensarlo dos veces, convocó a un equipo de 500 personas para trabajar en una vacuna. El jefe autorizó el pago de horas extras y hubo empleados que cancelaron sus vacaciones. Nacía el “Proyecto Velocidad de la Luz”.
BioNTech decidió apelar a una tecnología que nunca había sido aprobada para su uso en personas, la del ARN mensajero (ARNm) desarrollada por Katalin. En el inicio fueron seleccionadas 20 candidatas a vacuna, y comenzaron los test en roedores. Pero la compañía carecía de experiencia y recursos para encarar un gran ensayo clínico. Por eso Sahin llamó a Pfizer (venían trabajando juntos con tecnología de RNA desde 2018 en una vacuna contra la gripe) y habló con Kathrin Jansen.
“¿Creés que Pfizer querría trabajar en esta vacuna con BioNTech?”, le preguntó. “Desde luego. En realidad, yo misma estaba a punto de llamarte”, le respondió ella, a la velocidad de la luz. Ese diálogo fue el punto de partida para reorientar las investigaciones conjuntas hacia el virus flamante. Al día siguiente, las compañías acordaron asociarse en una vacuna contra el nuevo coronavirus mortífero. La noticia sería hecha pública a mediados de marzo, cuando la enfermedad se hacía fuerte en toda Europa y la Argentina estaba a un tris de comenzar su larga cuarentena.
Kathrin se puso a la cabeza de un equipo de 650 personas, en un esfuerzo vertiginoso y sin precedentes, para lograr una vacuna segura y eficaz. Sabía que estaba corriendo un gran riesgo con una tecnología no consolidada en el mundo científico, y que debía probar una nueva modalidad de inmunización y, a la vez, su eficacia contra este coronavirus específico. Pero ante el aumento vertiginoso de víctimas hizo todo lo posible por eliminar las trabas para su desarrollo, incluido el escepticismo inicial de sus colegas. Mantuvo la calma y recordó cómo, más de 15 años antes, había escuchado una amplia variedad de frases desalentadoras cuando trabajaba en su éxito contra el VPH. “Había mucha gente que pensaba que no iba a funcionar, y desde luego, estaban equivocados”, dijo. De manera similar, ahora tuvo confianza en una generación totalmente distinta de vacunas. Llegaba bien curtida en encarar desafíos y enfrentar desconfianzas. Lo demuestra su rica trayectoria científica.
Se formó en la Universidad Phillips de Marburg, donde asistió a las clases del reconocido biólogo Rudolf Thauer. Y en el mismo instante en que se doctoró -en microbiología, bioquímica y genética- aprendió por las malas el valor científico del fracaso: al terminar su tesis creyó que había descubierto una nueva vía química en las bacterias, pero en el experimento final sus resultados se desmoronaron. Fue una lección valiosa para su futuro en el desarrollo de drogas, donde la tasa de error es del 90% de las técnicas que se prueban.
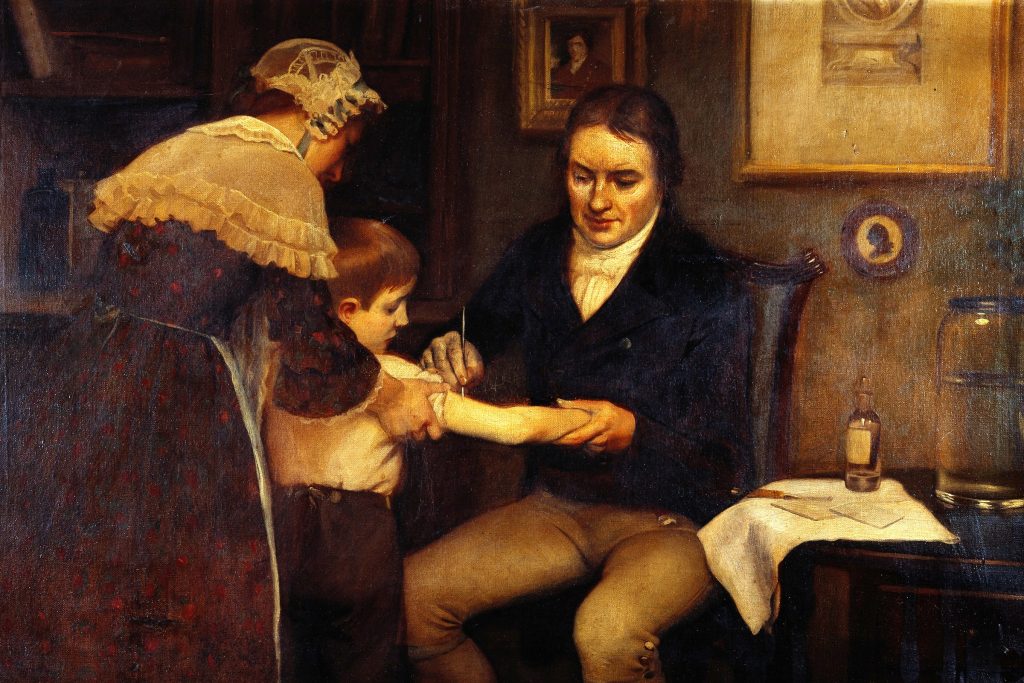
Tras un paso breve por Estados Unidos -una beca posdoctoral en la Universidad de Cornell en Ithaca, y otra en el Hospital General de Massachusetts- volvió a Europa para unas prácticas en el laboratorio de la Universidad de Oxford y para su primer trabajo en un gigante farmacéutico: el Instituto de Biología Molecular de Glaxo, en Ginebra. Ahí conoció a Alan Shaw, quien luego pasó a Merck y la invitó a trabajar en la división de vacunas de la empresa, de vuelta en Estados Unidos, en 1992. En Merck se zambulló en un proyecto que sus colegas consideraban una locura: el VPH, que a comienzos de los 80 se identificó como causa del cáncer de útero.
Merck ya había trabajado en la modificación de un virus para hacer una vacuna: la de la hepatitis B. Pero -recordó Edward Scolnick, encargado de los laboratorios de investigación de la compañía entre 1985 y 2002- no estaban interesados: otro laboratorio acababa de fracasar en la búsqueda de una vacuna contra el herpes y el VPH era muy difícil de investigar, sobre todo porque no se podía cultivar in vitro.
Kathrin insistió, Scolnick le pidió datos, y ella le entregó una cantidad de artículos científicos para leer. A la semana estaba convencido. Sólo necesitaría algunos ensayos previos para justificar el proyecto, le dijo, y ella se comprometió a completarlos de inmediato. “Es intrépida a la hora de asumir cualquier proyecto que considere de importancia, y no teme lanzarse de cabeza e ir averiguando qué hay que hacer”, la describió a la revista médica Stat. “En esta industria no es siempre así, porque muchos proyectos fracasan y la gente se preocupa por su empleo, si los bajarán de categoría, si los despedirán, si los pasarán por encima. Ella simplemente no piensa en eso”.
Durante el proceso Kathrin enfrentó el escepticismo de sus colegas en Merck, y también acusaciones de dilapidar recursos y hasta gritos en los pasillos. Pero en 2002, un ensayo en 2.400 mujeres mostró que una vacuna contra una cepa de HPV tenía una efectividad del 100%, y cuatro años más tarde Gardasil recibió aprobación de las autoridades sanitarias. Entre esas fechas, en octubre de 2004, Kathrin dejó Merck al cabo de 12 años en los que fue responsable también de vacunas contra el rotavirus, el herpes zoster, las paperas, el sarampión y la rubeola.
“Con una intuición científica y cuidado en los experimentos, tienes que seguir tu instinto y no permitir que los opositores te saquen de tu camino”, dijo mientras se sumaba como directora científica a VaxGen, una biofarmacéutica de San Francisco conocida por el fracaso de una vacuna contra el VIH. Después del 11 de septiembre de 2001 la empresa había recibido un contrato de 877,5 millones de dólares del gobierno de los Estados Unidos para producir 75 millones de dosis de una vacuna contra el ántrax. El bioterrorismo sería el campo de Kathrin por un tiempo, pero esa vez hubo fracaso: no fue posible mantener la vacuna químicamente estable.
En julio de 2006 pasó a Wyeth (con sede en Madison, Nueva York) como vicepresidenta senior para volver a sumergirse en un campo nuevo: las vacunas para niños. Emilio Emini, un ex jefe de ella en Merck, la convocó a trabajar en una de las “joyas” de la compañía: Prevnar. Desde su éxito médico y comercial en 2000, esa vacuna había logrado que las tasas de enfermedades por el neumococo, como neumonía, infecciones sanguíneas y meningitis, se redujeran en un 80% para los niños de menos de cinco años. Era eficaz en siete cepas de la bacteria; sin embargo, otras más raras, incluida la virulenta 19a, eludían su acción. Wyeth trabajaba en Prevnar 13, una versión contra 13 cepas del neumococo.
Ella llegó, estudió el trabajo hecho hasta el momento, y le preguntó a Emini: “¿Tenías idea de hasta qué punto esta situación es mala?”. Fue una pregunta sin queja, de mera curiosidad; a continuación, Kathrin puso manos a la obra. Emini -quien dirige el desarrollo global de vacunas en la Fundación Bill & Melinda Gates- admitió en fecha reciente a Stat: “Honestamente, no creo que hubiéramos podido tener éxito sin Kathrin”.
Pfizer compró Wyeth en 2009,por 68.000 millones de dólares. A la gran farmacéutica le faltaba una división fuerte de vacunas propias, y Prevnar 13 ocupó ese vacío al ser aprobada en 2010 para niños y para prevenir la neumonía en adultos mayores en 2012. Hoy es la vacuna más vendida en el mundo (facturó 5.800 millones de dólares el último año).
Con esta rica mochila de frustraciones y batallas ganadas -y una década transmitiendo su experiencia como profesora en la Universidad de Pensilvania- Kathrin encaró en marzo el desafío del Covid-19 desde su casa de Manhattan, confinada por la pandemia: intercambiaba innumerables llamadas diarias con su gente de Pfizer y con el equipo de BioNTech. Así coordinó las pruebas de las candidatas potenciales y llegó a competir cuerpo a cuerpo con el otro laboratorio que parecía avanzar más rápido, Moderna.
“Ella no sacrificaría la calidad por la velocidad”, explicó William Gruber, un ejecutivo histórico de Pfizer. “Es una académica realmente intransigente en lo que respecta al desarrollo de vacunas”, citó a su vez el experto Matthew Herper.
Aunque se jugaba un negocio anual multimillonario con muchos interesados -a mediados de enero de 2021 eran 91 las vacunas en estudio en el mundo, 20 de ellas en fase III-, Kathrin mantuvo un dominio firme de la operación, consciente de que tardara lo que tardase sería un récord. Se concentró, según su costumbre, en los datos. “Ella es exactamente la persona a la que uno querría en ese puesto”, la describió Paul Offit, director del Centro de Educación sobre Vacunas del Hospital de Niños de Filadelfia.
Al final, la conquista llegó en tan solo 210 días, desde el comienzo de las pruebas en abril hasta la finalización de los ensayos clínicos de fase III en noviembre.
La hoja de ruta en esos cinco meses de dientes apretados arrancó con ensayos iniciales en humanos, que detectaron dos candidatas finalistas a la vacuna conunapotente respuesta inmunológica. Se eligió la que tenía menores efectos secundarios para iniciar un estudio amplio y en varios frentes geográficos, con más de 30.000 voluntarios en Estados Unidos, Argentina (en el Hospital Militar), Brasil y Alemania. En septiembre se expandió el ensayo a 44.000 participantes.
El lunes 9 de noviembre, cuando Pfizer anunció que su vacuna contra el Covid-19 mostraba altísima efectividad, la esperanza del fin de la pandemia empezó a asomar en el horizonte. El mundo entero comenzó a hablar del gigante farmacéutico. Nadie, todavía, había reparado en Kathrin Jansen, la microbióloga que encabezó el logro, a la que el tiempo, una vez más, le daba la razón.
Mucho menos se reparó en la otra Catalina contemporánea de esta historia, Katalin Karikó, la “madre” de la vacuna, que aquel día pudo superar la taquicardia de la alegría pero decidió no celebrar: “Festejaremos todo esto cuando los sufrimientos humanos queden atrás, cuando los retos y este período terrible que vivimos tengan fin. Entonces lo celebraré verdaderamente”.
Crónicas

El Coronel no tiene quien le escriba
El misterio del supuesto militar que manejó la carrera de Elvis Presley y lo convirtió en el cantante más famoso de su época. ¿Quién era Tom Parker? ¿Era militar? ¿Era un agente encubierto de la CIA? O era simplemente un impostor.

El mito del voto latino
La última contienda electoral nuevamente mostró la necesidad de diversificar las opiniones en las redacciones. La reportera de ProPublica y el Texas Tribune, Perla Trevizo, explica por qué los medios deben poner atención a las diversas comunidades día tras día, no solo antes de las elecciones.

“Los humanos somos seres esencialmente artificiales”
Una conversación con Roger Bartra, el antropólogo y sociólogo mexicano, referente del pensamiento latinoamericano. Su especialidad, el estudio de la mutación de las especies.

“La sociedad digital no tiene límites. Hay que abrirse al mundo, verlo como un mercado único”
“Tenemos que generar energía en el cuerpo humano para alimentar pequeños dispositivos eléctricos” afirma Alliance Niyigena, de nacionalidad noruega, nacida en Ruanda y dedicada a la investigación en nuevas fuentes de energía. Tiene 25 años, es exponente de una generación diversa, sin moldes ni atavismos, abierta al mundo, que se preocupa de su cuidado porque es el espacio común.







